毛晓韵医生的科普号
- 精选 中国医大一院病志复印流程
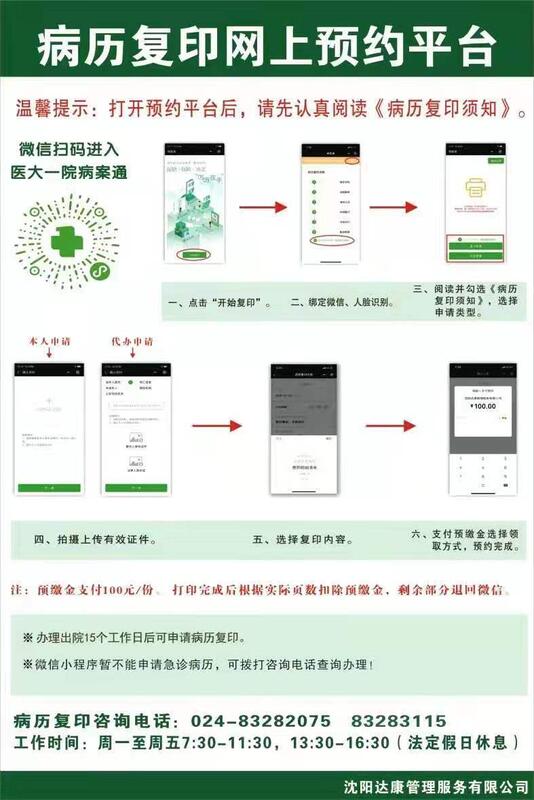 毛晓韵 主任医师 中国医大一院 乳腺外科1519人已读
毛晓韵 主任医师 中国医大一院 乳腺外科1519人已读 - 精选 中国医大一院乳腺就诊小TIP
1中国医科大学附属一院本部门诊位于沈阳市和平区南京北街155号,中山广场旁。2、门诊位于5楼和3楼,固定有5楼D区14诊室,D区21诊室,C区5诊室,3楼F区B304诊室。可先于网上挂号或者窗口挂号,然后到医院后,先扫码报道(如果不报道,医生电脑上显示不出患者的名字和信息),然后等待叫号。3、彩超位于四楼彩超中心,钼靶位于2楼钼靶室。大夫开完彩超后,可用手机交费(所有的收款台也可以交费),如行彩超,手机交费患者可收到电脑预约排位的彩超检查时间,收款台交费患者则去四楼可看到电脑预约排位的彩超检查时间,如预约时间来不了或想找某个老师做彩超,于四楼彩超中心人工预约处预约。预约钼靶,需去2楼预约。4退费流程:1)先于服务台打出发票,让医生签字盖章;2)再麻烦服务台帮助电脑上取消项目;3)收费处退费。如果需要办理入院,办理入院须知:非沈阳市医保患者,带中国医大一院乳腺外科挂号票(任何一天的任何医生的都行),沈阳市医保患者,带中国医大一院乳腺外科挂号票(任何一天的任何医生的都行,要带医保的挂号票,如果没挂,需要挂一下),先去乳腺外科医生办公室,开入院通知书后再去一楼出入院办理处交钱办理入院,回乳腺外科护士先接诊,医生接诊。非沈阳市医保患者入院,如果想走医保建议回当地办理转院手续,具体报销多少根据当地医保政策,各个城市不一样,不同类型医保也不一样。
毛晓韵 主任医师 中国医大一院 乳腺外科5932人已读 - 学术前沿 [ASCO2016]年轻女性乳腺癌患者生育热点问题回顾
毛晓韵 金锋 中国医科大学附属第一医院乳腺外科生育对患者治疗意愿的影响 一项多中心前瞻性队列研究入组了620例新近诊断为乳腺癌且年龄≤40岁的年轻女性患者,中位年龄为37岁。入组患者中68%在治疗前就与医生讨论了治疗对生育功能的影响,51%关注不孕的可能性。因为担心不孕,1%的患者拒绝化疗,1%的患者考虑不接受内分泌治疗,3%的患者拒绝内分泌治疗,11%的患者考虑少于五年的内分泌治疗,10%的患者接受了生育功能保护治疗。挪威一项以癌症人群为基础的队列研究发现,在各肿瘤患者中乳腺癌、宫颈癌和白血病患者生育的可能性最小。医生对生育及相关后果的认识 意大利一项162位肿瘤医生对乳腺癌患者生育问题态度调查结果表明,91%的肿瘤医生认为这个问题很重要,83%的肿瘤医生认为雌激素会刺激潜在的激素受体阳性肿瘤细胞生长,40%的肿瘤内科医生认为生育可能会增加激素受体阳性乳腺癌的复发风险,部分怀孕的乳腺癌患者会因为担心怀孕增加乳腺癌复发转移风险被主动流产。目前大多数针对年轻乳腺癌女性的生育功能的研究都集中在长期生存方面,很少涉及到其生育功能保护对乳腺癌治疗决策的影响或者是生育功能保护的策略的调整。怀孕是否会增加激素受体阳性乳腺癌复发转移的风险?——安全但不应鼓励 2011年Azim教授在Eur J Cancer杂志上发表的一篇荟萃分析研究分析了源于14项研究的确诊乳腺癌后的生育安全性,研究发现确诊乳腺癌后怀孕组较未孕组复发率降低41%(PRR=0.59,95%CI=0.5-0.7),特别是在淋巴结阴性的乳腺癌,亚组分析发现确诊乳腺癌后怀孕组和对照组两组总生存(OS)无明显差异。 2013年Azim教授在J Clin Oncol杂志上发表了一篇关于激素受体情况是否影响确诊乳腺癌后怀孕患者预后的多中心回顾性研究,入组条件为确诊乳腺癌1年以上、在怀孕前无复发转移证据,分为怀孕组(确诊乳腺癌后怀孕)和对照组,研究发现怀孕并不影响激素受体阳性组(HR=0.91,95%CI=0.67-1.24,P=0.55)和激素受体阴性组(HR=0.75,95%CI=0.51-1.08,P=0.12)患者的无病生存率(DFS)。乳腺癌治疗后的足月妊娠可以降低乳腺癌的相对死亡风险,即使是出现自然流产也能获得类似的获益,但人工流产对预后没有明显影响,且激素受体情况对OS的影响没有统计学意义(P=0.11)。怀孕似乎不能增加激素受体阳性乳腺癌复发转移风险。因为怀孕而中断内分泌治疗是否安全?——尚无证据 Azim教授总结了来自美国、加拿大、欧洲、中东和澳大利亚5个地区的数据发现超过50%的乳腺癌患者更愿意“一旦怀孕就中断内分泌治疗”,但安全性目前尚无定论。国际乳腺癌研究组(IBCSG)组织的一项旨在探讨因为怀孕而中断内分泌治疗安全性和获益研究——“POSITIVE研究”正在展开。LHRH抑制剂是否可以减轻化疗引起的卵巢功能损害? 2007年Hum Reprod发表的文章表明化疗能导致卵泡的破坏、减少以及卵巢血管透明变性,间质的纤维化,最终出现卵巢重量减少储备功能下降,甚至卵巢萎缩等,促性腺激素的增加和雌二醇水平降低。近年来研究表明化疗可以将绝经时间提前约10年,近几年来4篇关于LHRH抑制剂防止化疗引起卵巢功能损害的文章结果是不一致的。2011年Del Mastro L发表于JAMA杂志的PROMISE-GIM6研究显示化疗联合使用LHRHα暂时性抑制卵巢功能,可使早期绝经前乳腺癌患者早发性卵巢功能衰竭的发生率降低17%。2011年Gerber B在J Clin Oncol杂志上发表了GBG 37 ZORO研究结果,这项研究纳入60例小于46岁激素受体阴性的乳腺癌新辅助化疗患者,部分患者同时随机加用LHRH抑制剂,结果发现LHRH抑制剂的卵巢功能保护作用缺乏临床和统计学意义。2012年Munster PN在J Clin Oncol杂志上发表了一项前瞻性随机对照研究用于评估LHRH抑制剂用于早期乳腺癌化疗时对卵巢功能保护作用,以月经的恢复为终点指标,结果显示LHRH抑制剂组与对照组在化疗后月经恢复的比例与中位月经恢复时间没有差别。 2015年发表于《新英格兰医学杂志》的POEMS研究结果显示,对于激素受体阴性乳腺癌患者,化疗结束2年时的卵巢早衰率在化疗+LHRH抑制剂组为8%,显著低于单纯化疗组的22%,且与化疗联用不影响化疗的疗效。 2015年Lambertini发表于Ann Oncol杂志的荟萃分析得出的结论也是化疗联合使用LHRH抑制剂对防止化疗引起的卵巢功能损害是有保护作用的,可以减少卵巢早衰的发生风险。LHRH抑制剂可以降低化疗带来的闭经,停药后月经仍然可以来潮,后续月经恢复并不代表生育能力的完全恢复,LHRH抑制剂对后续月经恢复后绝经年龄的影响或卵巢储备的影响尚不清楚。虽然且LHRH抑制剂组怀孕率明显高于对照组,但是数量相差不多。Azim教授认为,LHRH抑制剂可以降低化疗带来的闭经,对于有生育意愿但不愿意进行辅助生殖的患者来说不失为一个选择。小结 综上,2016ASCO大会上的探讨为年轻女性乳腺癌患者的生育安全性打开了一扇窗,目前研究都是针对早、中期乳腺癌患者,大多为回顾性研究。我国近几年来年轻乳腺癌患者比例持续增加,不久的将来年轻乳腺癌患者可能更多是独生女,乳腺癌后生育问题更应被极早研究和加以关注,目前也尚无系统性中国年轻乳腺癌患者生育安全性的研究数据。确诊乳腺癌后患者生育需要考虑各种危险因素,因为部分高危乳腺癌患者一旦在妊娠中复发转移带来的创伤可能是加倍的,还要充分考虑妊娠过程的管理、治疗对胎儿的影响和后续的治疗方案等。最佳的生育方案是由肿瘤复发风险、患者一般情况、经济情况及个人意愿共同决定的,需要肿瘤科、妇科、产科、辅助生育等学科共同参与、指导与跟进。
毛晓韵 主任医师 中国医大一院 乳腺外科1957人已读 - 学术前沿 “精准、决策和切口“--乳腺导管内癌局部处理的热点问题
毛晓韵 金锋 中国医科大学附属第一医院乳腺外科 热点一:DCIS是否需要术后放疗 随着时代进步,乳腺癌手术治疗的时机和范围有很大的改变,手术范围小了但更加精准了。目前的趋势是本着安全的原则,能少切就不多切。对于DCIS的局部处理,4个大型随机性试验证明了保乳术+术后放疗可以大幅降低局部复发率,虽然局部复发患者都是浸润性病变,但预后与是否辅助化疗无关。目前临床上是以肿瘤学分级、肿瘤切缘是否阳性、激素受体情况、年龄、肿物的触诊情况等,以及与临床和病理相关的van nuys 预后因素和MSKN指数作为导管内癌术后放疗风险评估指标。 来自瑞典的一项研究纳入了379例钼靶阳性表现的DCIS患者,切缘阴性,术后按其危险因素决定是否放疗,根据激素受体表达情况,25%的患者术后接受了内分泌治疗。研究者通过组织化学方法检测了p16、Ki-67、COX-2、PgR、FOXA1和SIAH2的表达,通过原位杂交检测HER-2是否扩增。研究发现患者DCIS原发灶的病理学分级或肿物大小均不能改变术后发生浸润性病变的风险,但全乳房放疗可以明显降低这种风险。如未放疗,p16、Ki-67、COX-2、PgR、FOXA1、SIAH2和HER-2分子生物学标志对术后浸润性病变复发风险有良好的预测。 旨在探讨低风险DICS是否需行放疗的RTOG9804试验入组了1790例T<2.5 cm、切缘>3 mm的低或中等级的DCIS患者,将其随机分为术后放疗组和对照组,随访中位时间为7年,受试者平均年龄为58岁。术后放疗组局部复发率为0.9%,对照组局部复发率为6.7%,两组的复发率都不高,但放疗组的局部复发率更低,差异有统计学意义。DCIS本身的复发风险不高,似乎仅对复发风险高的患者进行放疗,可以进一步提高低风险患者的生存质量。在未来的研究中,能否将分子生物学标志物作为放疗危险因素进行评估后再有选择地进行放疗,是我们需要探讨的问题。 另一项ECOG5194试验也报道了低风险DCIS患者术后仅行观察的前瞻性试验结果,这项单臂研究将切缘≥3 mm的DCIS患者分为两组,低或中级别DCIS且T≤2.5 cm归入组1,高级别DCIS且T≤1.0 cm归入组2,两组患者均不放疗。中位随访12年,研究者发现组1的局部复发风险为14.4%,组2的局部复发风险为24.6%。虽然在这些试验中局部复发和总生存不同,但可以明确的是放疗可以降低局部复发和增加总生存,“本着安全的原则,是否放疗可以根据危险因素综合判断,以实现个体化”,这也体现了此次ASCO会议上“个体化精准”治疗的主旨。 热点二:导管内癌患者保乳手术切缘要多大才安全? 乳腺癌保乳手术安全切缘的定义一直存在争议,切缘阳性会增加术后局部复发率,但若切除范围过广,则会影响术后乳腺外形。阳性切缘二次切除目前是不提倡的,因为其增加了外科并发症、影响保乳术后外观,增加费用和患者焦虑程度。DCIS患者保乳手术的安全切缘目前仍没有明确的标准。 一项DCIS患者保乳手术切缘与局部复发关系的荟萃分析研究纳入了20个研究共7883例行保乳手术的DCIS患者,中位随访时间78.3个月,其中71%的患者接受了术后放疗。研究结果发现增加切缘的距离并不能进一步降低局部复发率。Dunne等的研究发现>2 mm的切缘局部复发率差异没有统计学意义,但在入组的所有研究中,>10 mm的切缘其术后局部复发率是最低的。只有5项研究纳入了>10 mm的切缘。DCIS患者保乳手术的安全切缘目前仍没有明确的标准,需要更多的临床证据来明确在何种切缘宽度下DCIS患者获益最大。保乳手术联合放疗能显著降低DCIS的局部复发,是大部分患者可选择的局部治疗方式。目前倾向于针对接受保乳手术且术后拟行放疗的DCIS患者,2 mm是较为适当的手术切缘宽度,但该观点是否客观,仍需要探讨。 “患者依从性”在整个治疗过程中有举足轻重的地位,医生应与患者讨论各项手术方案的利弊,制定术后辅助治疗及随访策略,最佳的治疗方案是由肿瘤复发风险、患者一般情况、经济情况及个人意愿共同决定的。
毛晓韵 主任医师 中国医大一院 乳腺外科2628人已读 - 学术前沿 延长内分泌治疗如何更精准?
[ASCO2016]金锋:延长内分泌治疗如何更精准——可手术ER阳性乳腺癌5年内分泌治疗预后相关因素研究中国医科大学附属第一医院乳腺外科毛晓韵发自美国芝加哥ASCO2016现场,金锋审阅 5年的内分泌治疗可以降低可手术的ER阳性乳腺癌术后0~4年和5~14年两个阶段的乳腺癌死亡率,这项纳入46 138例可手术ER阳性乳腺癌(肿物≤5 cm,淋巴结状态为N0,N1-3 或N4-9)的研究发现,肿物大小和淋巴结状态是5年内分泌治疗后乳腺癌复发转移的影响因素,肿瘤分级、Ki-67、孕激素受体(PR)和人表皮生长因子受体(HER-2)状态也是有影响的。 淋巴结有1~3枚转移的患者相对于淋巴结没有转移的患者,远处复发的相对危险度(RR)为2.08(95%CI:1.87-2.32);T2N0患者相对于T1N0患者,远处复发 RR为1.73(95%CI:1.53-1.95);在T2N0患者中,肿瘤病理分级高的患者相对于分级低的患者,远处复发RR为2.02(95%CI:1.44-2.83);Ki-67表达>20%的患者相对于Ki-67表达<13%的患者,远处复发RR为1.63(95%CI:1.23-2.16)。同样以上因素对于乳腺癌死亡率也是有影响的,而对侧乳房乳腺癌复发率受影响甚微(0.3%/年)。 该研究提示我们,尽管ER阳性乳腺癌经5年内分泌治疗后其术后5~14年的复发风险是稳定的,T分期和N分期越早、肿瘤病理分级越低,复发风险也越小,但就算是低级别的T1N0患者也存在一定的复发转移风险。 ER阳性乳腺癌内分泌治疗,5年还是更长?早在2013年《柳叶刀》上发表的ATLAS试验结果就已表明:与5年相比,术后接受他莫昔芬辅助内分泌治疗10年更能使ER阳性的乳腺癌患者受益。这项纳入1996-2005年全球12 894例早期乳腺癌患者的研究结果表明,他莫昔芬10年组vs. 他莫昔芬5年组复发风险RR为0.84(95%CI:0.76–0.94),且内分泌治疗10年组乳腺癌病死率和总病死率均明显小于5年组。其进一步的研究表明确诊乳腺癌10年后,他莫昔芬 10 年组vs. 他莫昔芬5年组累积复发风险RR为0.75(95%CI:0.62-0.90),这种获益在确诊乳腺癌10年后更加明显。 所有内分泌治疗的患者肺栓塞RR为1.87(95%CI:1.13-3.07)、卒中RR为1.06(95%CI:0.83-1.36)、缺血性心脏病RR为0.76(95%CI:0.60-0.95)以及子宫内膜癌RR为1.74(95%CI:1.30-2.34)。子宫内膜癌在5~14年的累积危险度在继续治疗组为3.1%(致死率0.4%),对照组为1.6%(致死率0.2%,致死率较对照组增加0.2%)。 10年他莫昔芬治疗会增加子宫内膜癌风险,以前的ASCO会议也对此议题也有过深入的探讨,其结论为ER阳性乳腺癌患者确诊5年后复发概率较高,虽然延长辅助治疗增加了副作用,但延长内分泌治疗的获益还是肯定的,特别是后续效应的获益。延长辅助内分泌治疗疗程成为可选临床方案,尤其使年轻患者长期额外获益。 本次ASCO大会上Hongchao Pan的报告主要为了解决哪些因素是低风险患者5年内分泌治疗后需要延长治疗时间的危险因素,研究表明肿物大小和淋巴结状态是5年内分泌治疗后乳腺癌复发转移的影响因素,肿瘤分级、Ki-67、PR和HER-2状态也是有影响的,越早的T和N分期和肿瘤病理分级越低,其复发风险也越小,但就算是低级别的T1N0患者也存在一定的复发转移风险。本次ASCO大会对乳腺癌内分泌治疗从5年延长至10年有一个精准推进。在临床实践中,临床医生应具体问题具体分析,根据患者危险因素综合考虑后制定最佳的个体化治疗方案。 金锋 教授 教授 主任医师 博士研究生导师,中国医科大学附属一院乳腺外科主任,中国临床肿瘤学会(CSCO)执行委员,中国抗癌协会乳腺专业委员会常务委员,中国老年学学会乳腺癌分委会副主任委员,中华医学会肿瘤学分会乳腺癌学组委员,中国医师学会乳腺癌专业委员会常委,辽宁省抗癌协会理事,辽宁医学会肿瘤分会副主任委员,辽宁医学会外科分会乳腺外科学组组长。
毛晓韵 主任医师 中国医大一院 乳腺外科1442人已读 - 学术前沿 SUPERMO临床试验中病理质控的重要性
SUPERMO(乳腺癌乳房切除术后放疗选择性应用的临床试验)是一项III期的多中心随机对照临床试验,其用于评估中危可手术乳腺癌患者行全乳房切除术后胸壁辅助放疗的作用。这项临床试验由英国爱丁堡大学发起,16个国家共1688位乳腺癌患者入组。其将入组患者中危因素定义为如下:1)T1-2pN1M0患者;2)T2pN0病理组织学分级III级或/和淋巴管侵犯阳性患者;3)T3pN0患者。 目前SUPERMO试验的病理质控报告指出,研究中心的两位病理医师对参与此项临床试验患者乳腺癌原发灶及淋巴结切片进行病理复审,单盲阅片以得出关于肿瘤类型、组织学分级和淋巴结转移情况与入组时分中心一致的结论。在此项临床试验中,两个大的分中心英国和冰岛共入组此研究85%的患者(英国入组患者占75%,冰岛入组患者占10%),不同国家的分中心在组织学III级和淋巴管侵犯阳性患者占入组患者的比率无明显统计学差异,其中1215位为淋巴结转移阳性,414位为淋巴结转移阴性的乳腺癌患者。82.0%(1369例)的入组患者参与了此次病理复审,其中963位为淋巴结转移阳性,406位为淋巴结转移阴性的乳腺癌患者。其中104例淋巴结转移阴性患者在分中心不满足中危因素的组织学分级或淋巴管侵犯要求归为非中危因素组,但在此次病理复检中在组织学分级或淋巴管侵犯方面满足了中危因素,拟将其归为中危因素组。考虑到入组的严谨性,研究组让病理医生对此部分病例再次进行在线病理评估并得出一致性结论后,这个数由104例减少到70例。 来自最大的英国分中心数据表明,41.2%患者存在淋巴结侵犯阳性和54.6%患者组织学分级为III级,而研究组复审数据表明15.1%患者存在淋巴结侵犯阳性和42.4%患者组织学分级为III级,分中心的这两组数据与研究组复审的数据存在明显统计学差异(均P≤0.0001)。在此项临床试验中组织学分级和淋巴管侵犯的准确评估非常重要,其关系到病例的入组,对SUPERMO临床实验结果有举足重轻的影响。 SUPERMO临床试验旨在评估中危的可手术乳腺癌患者术后行胸壁辅助放疗的必要性,此试验的结果对于我们未来对肿物为T2且无淋巴结转移的患者是否进行放疗有重要意义,其在实验设计时认为病理组织学分级III级和淋巴管侵犯阳性是预后差、需要放疗的危险因素,将来病理组织学分级和淋巴管侵犯也许会像淋巴结转移一样作为评估患者预后和指导治疗的重要因素,但现阶段来说一致的评估标准和客观的准确评估是重点,研究者也推荐病理切片扫描技术的大规模应用,这对组织学分级和淋巴管侵犯的准确病理评估是大有裨益的。
毛晓韵 主任医师 中国医大一院 乳腺外科1685人已读 - 学术前沿 三阴性乳腺癌的春天?卡培他滨联合用药治疗中高危早期乳腺癌
该研究共入组1500例淋巴结转移阳性或淋巴结阴性但复发风险高的乳腺癌患者。入组标准:病理确诊为中高危复发风险的浸润性乳腺癌,区域淋巴结转移阳性或肿瘤直径>2cm,同时PR阴性。其他入组标准包括:18-65岁,体能状态评分0或1,术后心肝肾功能正常且不存在远处转移,未接受新辅助化疗。患者随机分入卡培他滨组(3TX-3CEX化疗)和对照组(3T-3CEF),主要研究终点为无复发生存(RFS),次要研究终点包括安全性和总生存。试验设计如图1。图1. FinXX研究试验设计 该研究中位随访59个月的结果在2012年的Journal of Clinical Oncology杂志上发表。当时两组共发生215例局部及远处复发,卡培他滨组96例,对照组118例,但组间RFS无明显差异(HR=0.79;95%CI,0.60-1.04;P=0.087;5年RFS:卡培他滨组86.6% vs.对照组84.1%)。卡培他滨组有56例乳腺癌相关死亡,对照组75例(HR=0.73;95%CI,0.52-1.04;P=0.080)。探索性数据分析发现卡培他滨组可以增加三阴性乳腺癌和淋巴结转移3枚以上乳腺癌的OS和RFS,且两组患者在严重副作用发生率方面无统计学差异。 这次ASCO大会报道了FinXX试验十年生存分析结果和乳腺癌分子分型亚组分析结果。此次中位随访时间为10.3年,两组共发生303例局部及远处复发,卡培他滨组142例,对照组161例,组间RFS差异无统计学意义(HR=0.85;95%CI,0.680-1.07;P=0.1687)。卡培他滨组有120例乳腺癌相关死亡,对照组141例(HR=0.83;95%CI,0.65-1.06;P=0.132),两组OS无显著差异。两组患者对侧乳腺癌发生率和其他肿瘤发生率差异无统计学意义。亚组分析发现,在三阴性乳腺癌亚组中,卡培他滨组的RFS(HR=0.43;95%CI,0.24-0.79;P=0.007)和OS(HR=0.55;95%CI,0.31-0.96;P=0.037)明显优于对照组,而在其他亚组未发现此类优势(图2、图3)。图2. 不同分子分型亚组乳腺癌接受卡培他滨联合化疗的生存获益图3.三阴性乳腺癌亚组接受卡培他滨联合化疗的生存获益 在副作用方面,卡培他滨组在化疗相关中性粒细胞减少和中性粒细胞减少性发热方面均优于对照组(P值均<0.05),但卡培他滨组在可接受的副反应(腹泻和手足综合征)发生率均明显高于对照组。 这次ASCO大会报道了FinXX试验十年生存分析结果,且在亚组分析上有了更为精准的解读,其更适于三阴性乳腺癌的联合治疗,但此研究的三阴性乳腺癌患者入组例数有待增加,且这类探索性数据分析在概率意义上的精确性还有待提高,我们也期待更多卡培他滨在中国乳腺癌人群中的数据。不管怎样,此次ASCO大会给三阴性乳腺癌带来了春天的气息。
毛晓韵 主任医师 中国医大一院 乳腺外科3852人已读





